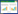文章信息
基金项目
- 2019年医疗服务与保障能力提升补助资金(中医药事业传承与发展部分)“全国中药资源普查项目”(财社〔2019〕39号);福建省科技厅引导性项目(2018Y0049);福建省卫生计生科研人才培养项目(2017-1-70,2016-2-28);福建省教育厅省属高校科研专项(JK2017024)
作者简介
- 温秀萍(1984—),女,硕士,助理研究员,研究方向为药用植物资源与种质选育,E-mail:375706654@qq.com.
文章历史
- 收稿日期:2021-03-04
2. 福建中医药大学附属泉州市正骨医院,福建 泉州 362000;
3. 福建中医药大学生物医药研发中心,福建 福州 350122
2. Quanzhou Orthopedic Traumatological Hospital of Fujian Traditional Chinese Medicine University, Quanzhou 362000, China;
3. Centre of Biomedical Research & Development, Fujian University of Traditional Chinese Medicine, Fuzhou 350122, China
【研究意义】绞股蓝〔(Gynostemma pentaphyllum(Thunb.)Makino〕为葫芦科绞股蓝属多年生草质攀援植物[1],是常用的中草药之一,又名五叶参、七叶胆。绞股蓝是除五加科植物外含有人参皂苷成分的药用植物之一,主要分布在湖南、云南、广西等省区,因此有“南方人参”的美称[2]。最早作为救荒的野菜食物记载于《救荒本草》 [3]。《中华本草》记载其以全草入药,味苦,微甘,性凉,归肺、脾和肾经,具有清热、补虚、解毒的功效,主治体虚乏力、虚劳失精。原中华人民共和国卫生部在2002年将绞股蓝列为可用于保健食品的药物之一;2017年福建省中药材产业协会将其列入“福九味”,作为福建省重点发展的中药材。目前,绞股蓝已有10余个省级中药材标准,但尚未收录于《中华人民共和国药典》(以下简称《中国药典》),其质量标准只有性状鉴别、显微鉴别,或水分、总灰分、浸出物含量测定,未能全面反映和评价绞股蓝的质量。
【前人研究进展】现代化学成分研究表明,绞股蓝主要含有皂苷类、黄酮类和多糖类成分以及多种氨基酸、微量元素和矿物质等[4-7]。药理研究表明,绞股蓝具有抗肿瘤[8]、镇静抗焦虑[9]、降血脂[10]、抗氧化以及延缓衰老等重要作用[11]。质量研究主要涉及农残、重金属、总苷提取物和总苷片制剂、配方颗粒[3, 12-16]等方面。近年来,绞股蓝的各种茶类饮料、口服液、养生酒以及食品添加剂等销售量巨大,但其质量控制体系还不够完善,关于药材中水分、灰分、浸出物含量的相关标准和研究较少。
【本研究切入点】水分、灰分等是影响中药材和代用茶质量的一个重要因素,水分超过一定范围容易在储藏过程中霉变、潮解,导致虫害或者变质[17]。为了能更安全有效地利用绞股蓝,本试验以不同产地的绞股蓝为研究对象,比较不同产地药用和茶饮绞股蓝的水分、灰分、酸不溶性灰分、水溶性浸出物的含量。【拟解决的关键问题】本研究通过评价不同产地药用和茶饮绞股蓝的质量,明确各质量控制项目的限量,以期为提升绞股蓝的质量标准提供参考。
1 材料与方法 1.1 试验材料试验样品:包括产自陕西、福建、广西、安徽、河北、江西等不同省区的绞股蓝样品(均被加工成药材或茶叶),购于安徽亳州、河北安国等多个药材市场,共计75批次,其中药用绞股蓝20批、茶饮绞股蓝55批(表 1)。供试样品存放于福建中医药大学中药资源标本馆,经福建中医药大学药学院范世明正高级实验师鉴定为绞股蓝。根据采摘部位不同,绞股蓝样品分全草、茎和叶、茎、叶、龙须(图 1、图 2)。全草即为绞股蓝的地上全草;茎和叶为绞股蓝距离地面15 cm以上的整株茎蔓;叶为绞股蓝整株茎蔓2/5~4/5之间的叶;龙须为绞股蓝顶尖6~12 cm的嫩芽尖(须叶完整、嫩茎尖);茎为绞股蓝整株茎。

|
| 图 1 药用绞股蓝的不同部位 Fig. 1 Different parts of medicinal Gynostemma pentaphyllum |

|
| 图 2 茶饮绞股蓝的不同部位 Fig. 2 Different parts of tea Gynostemma pentaphyllum |
主要试剂:5% 硝酸银水溶液(南京森贝伽生物科技有限公司),盐酸和无水乙醇(分析纯,国药集团化学试剂有限公司)。
仪器与设备:恒温水浴锅(苏州珀西瓦实验设备有限公司)、XM7D-8222型电热恒温干燥箱(上海精宏实验仪器厂有限公司)、SHB-Ⅲ循环水式多用真空泵(郑州长城科工贸有限公司)、BSA224S型万分之一分析天平〔赛多利斯科学仪器(北京)有限公司〕、KSW-4D-11箱式电阻炉(上海实验电阻炉)、调节式万用电炉(南通市长江光学仪器有限公司)、XS-05药材粉碎机(上海兆申科技有限公司)。
1.2 试验方法1.2.1 水分测定 采用《中国药典》(2020年版)四部通则0832中的烘干法测定绞股蓝样品水分。取绞股蓝样品约3 g,平铺于烘至恒重的称量瓶中,厚度不超过10 mm,精密称定,将称量瓶放入105 ℃烘箱中,瓶盖打开,干燥5 h后取出,移置干燥器中冷却30 min后,取出精密称定,再按上述方法进行干燥1 h,放冷,精密称重,计算两次称重的差异,直至连续两次称量差异不超过5 mg。平行操作3次,计算样品的含水量。
1.2.2 灰分测定 (1)总灰分:参照《中国药典》四部通则2302测定绞股蓝灰分。取绞股蓝粉末3 g,精密称定,置于炽灼至恒重的坩埚中,称定重量,置于电炉上缓慢炽热使样品充分炭化至无烟,注意避免燃烧。炭化后放入马弗炉中,在550 ℃下灼烧6 h,冷却至200℃后取出,放入干燥器中冷却30 min,准确称量。反复灼烧至前后两次称量差异不超过5 mg。平行操作3次,根据残渣重量,计算总灰分含量。
(2)酸不溶性灰分:取上述所得的灰分,根据《中国药典》四部通则2302测定酸不溶性灰分。在坩埚中加入稀盐酸10 mL,盖上表面皿,水浴加热10 min,表面皿用5 mL热水冲洗,洗液并入坩埚中,坩埚内的残渣用水洗于滤纸上,用蒸馏水反复洗涤至洗液中滴入硝酸银不变浑浊为止。将滤渣连同滤纸移置原坩埚中,在沸水浴上蒸干坩埚内水分,再移至马弗炉中炽灼5 h。待炉温降至200℃,取出坩埚,放入干燥器内冷却至室温,精密称定。重复操作直到前后两次称量差异不超过5 mg。平行操作3次,根据残渣重量,计算酸不溶性灰分含量。
1.2.3 浸出物测定 依据《中国药典》四部通则2201中的热浸法测定水溶性浸出物。精密称定绞股蓝粉末4.0 g,置250 mL锥形瓶中,添加蒸馏水100 mL,盖上瓶盖摇晃均匀,称定装有样品和试剂的锥形瓶,静置1 h后连接回流冷凝管,待水浴锅温度达到100 ℃后将试样加热至沸腾,并保持微沸1 h。取出锥形瓶盖上瓶塞放冷,补足失重,摇匀,用干燥滤器滤过。精密量取滤液25 mL,置于已干燥至恒重的蒸发皿中,水浴蒸干后,于105 ℃干燥3 h,置于干燥器中冷却30 min,迅速精密称定并记录数据,以干燥品计算供试品中水溶性浸出物的含量。
1.3 数据统计分析试验数据用Excel 2013进行整理,应用SPSS 19.0软件对不同产地绞股蓝的水分、灰分和浸出物含量数据进行统计分析,并通过绘制柱形图进行结果可视化展示。
2 结果与分析根据绞股蓝样品作用不同,分为药用和茶饮两种,药用绞股蓝共收集20批次样品,产于福建、安徽、湖北、广西、陕西、四川和云南,主要以全草为主,仅福建1批次药用部位为茎。茶饮绞股蓝共收集55批次样品,产于福建、安徽、甘肃、广西、贵州、湖北、吉林、江苏、陕西、江西、四川和云南,基本为茎和叶、叶,有6批次为龙须,仅吉林产地的2批次茶饮绞股蓝为全草。
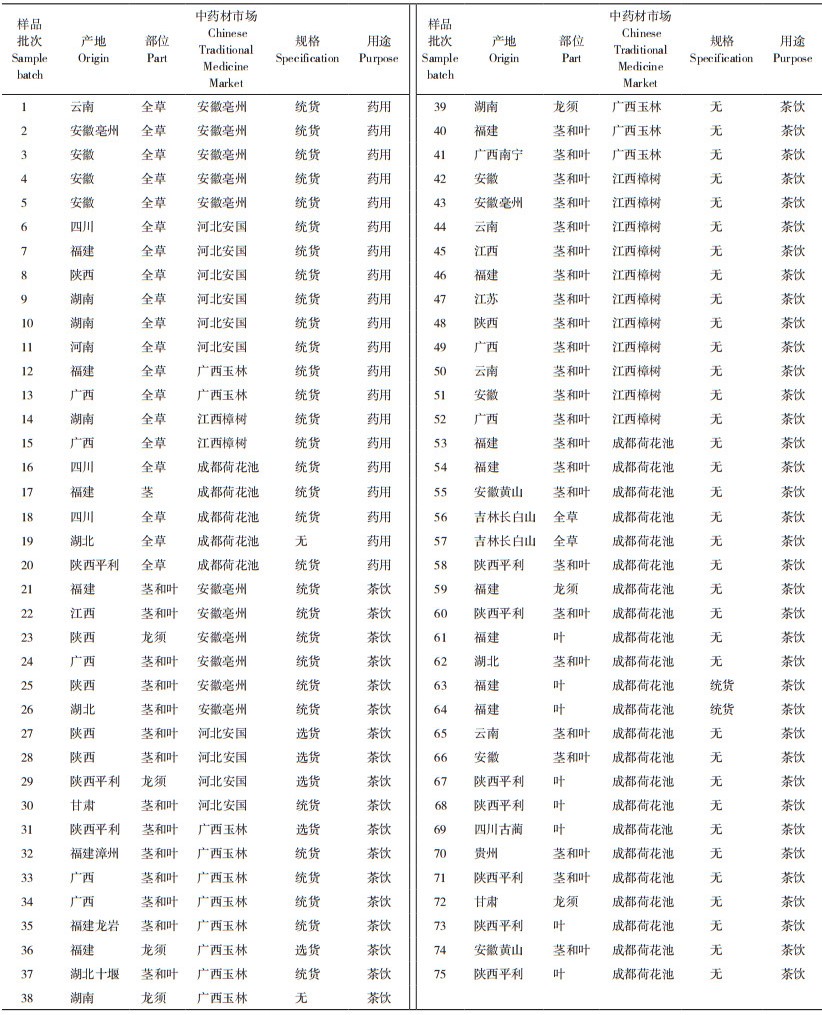
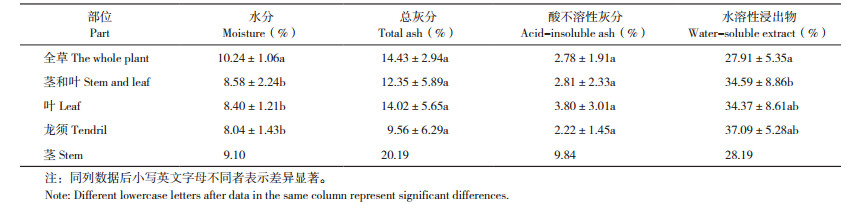
2.1 不同产地绞股蓝含水量分析根据供试绞股蓝水分测定结果,20批次药用绞股蓝样品中,含水量范围在8.31%~12.78% 之间,均值为10.29%。绞股蓝的部位不同,其含水量也不同,其中全草的含水量最高,与龙须、叶、茎和叶3种部位的含水量均具有显著性差异(表 2)。根据绞股蓝样品产地进行比较,结果(图 3)发现,全草类样品仅广西两批次的含水量超过12%,其他均在12% 以下,吉林和福建样品的含水量较低;茎和叶样品中,云南、江西、贵州和广西样品的含水量较高,陕西与湖北样品的含水量较低;在单纯的叶样品中,含水量从高到低分别为福建、四川和陕西样品;在龙须样品中,福建、甘肃、陕西和湖南样品的含水量逐渐降低;茎样品仅有福建1批次,含水量为9.1%。
|
|
| 图 3 不同产地绞股蓝不同部位的水分含量 Fig. 3 Moisture content in different parts of Gynostemma pentaphyllum from different origins |
2.2 不同产地绞股蓝总灰分含量分析
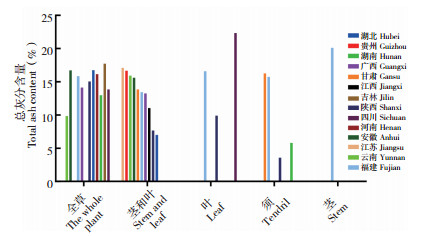
根据供试绞股蓝总灰分测定结果可知,不同产地20批次药用绞股蓝样品中,总灰分含量范围在9.41%~20.19% 之间,总灰分均值为14.39%。绞股蓝不同部位之间的总灰分含量无显著性差异(表 2)。但相同部位不同产地样品的总灰分差异较大,全草类样品中,以吉林样品的总灰分含量最高、为17.79%,而云南样品的总灰分含量最低、为9.9%;茎和叶样品中,江苏、贵州、云南和安徽样品的总灰分含量较高,超过15%,而陕西、湖北样品的总灰分含量均值低于8%;在单纯的叶样品中,含水量从高到低分别来源于四川、福建和陕西;在单纯的龙须样品中,福建和甘肃样品的总灰分含量较高,陕西和湖南样品的总灰分为20.19%(图 4)。
|
| 图 4 不同产地绞股蓝不同部位的总灰分含量 Fig. 4 Total ash content in different parts of Gynostemma pentaphyllum from different origins |
2.3 不同产地绞股蓝酸不溶性灰分含量分析
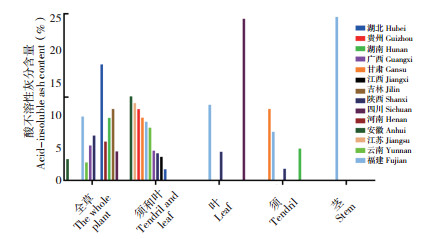
根据供试绞股蓝酸不溶性灰分测定结果,除部位为茎之外的19批次药用绞股蓝样品,其酸不溶性灰分含量范围在0.57%~6.99% 之间,均值为2.62%。绞股蓝不同部位之间的酸不溶性灰分含量无显著性差异(表 2)。全草类样品中,以湖北样品的酸不溶性灰分含量最高、为6.99%,其他样品含量均低于5%;茎和叶样品中,安徽样品的酸不溶性灰分含量均值最高,最低为湖北样品;在单纯的叶样品中,酸不溶性灰分含量从高到低分别为四川、福建和陕西样品;在单纯的龙须样品中,酸不溶性灰分含量从高到低分别为甘肃、福建、湖南和陕西样品;单纯的茎样品仅福建1批次,酸不溶性灰分为9.84%(图 5)。
|
| 图 5 不同产地绞股蓝不同部位的酸不溶性灰分含量 Fig. 5 Acid-insoluble ash content in different parts of Gynostemma pentaphyllum from different origins |
2.4 不同产地绞股蓝水溶性浸出物含量分析
根据供试绞股蓝水溶性浸出物测定结果,不同产地20批次药用绞股蓝样品的水溶性浸出物(热浸法)含量在20.86%~39.79% 之间,均值为27.92%。茎和叶样品的浸出物含量显著高于全草类样品,其他不同部位样品之间无显著性差异(表 2)。陕西样品在各个部位(除茎外)的浸出物含量均高于其他产地样品;此外在全草类中,广西、湖北和福建样品的浸出物含量较高,而安徽、云南和四川样品的含量较低;在茎和叶中,江西、湖北、甘肃和福建样品的含量也较高,而贵州和云南样品的含量较低(图 6)。

|
| 图 6 不同产地绞股蓝不同部位的水溶性浸出物含量 Fig. 6 Water-soluble extract content in different parts of Gynostemma pentaphyllum from different origins |
3 讨论 3.1 药用绞股蓝质量控制标准
中药材中含有较多亲水大分子,如蛋白质、多酚、糖类等,当其含水量超过15%,易引起霉变、酸败、虫害等情况,影响中药材的药用价值[18],而灰分含量能反映金属矿物质水平。目前省级中药材标准中,《福建省中药材标准》(2006年版)、《四川省中药材标准》(2010年版)、《广西壮族自治区瑶药材质量标准》(第一卷)、《江西省中药材标准》(1996年版)和《贵州省中药材民族药材质量标准》(2003年版)等均未有绞股蓝的质量控制指标及限量[19-24];《山东省中药材标准》(2012年版)、《山西省中药材中药饮片标准》(2017年版)、《湖北省中药材标准》(2009年版)、《湖南省中药材标准》(2009年版)和《香港中药材标准》(第五册)[25-29]5个省(区)有绞股蓝的质量控制限量,其中水分限量在10.0%~15.0% 之间,总灰分限量标准在10.0%~16.0% 之间(湖南省无),酸不溶性灰分最高限量为4.0%(湖南省无),热浸法水溶性浸出物最低限量为16.0%(湖南、湖北省无)。而本试验检测结果发现,供试的20批次药用绞股蓝的含水量基本在12.0% 以下,浸出物含量均在20.0% 以上,均符合标准要求;但有7批次的总灰分含量超过16.0%,基本涵盖每个省区的样品;有6批次的酸不溶性灰分含量超过最高限量(4.0%),14批次的酸不溶性灰分含量不高于3.0%。从上述数据可看出,目前有关绞股蓝药材质量控制指标的标准较少,而且部分限量要求较低,为进一步提升药用绞股蓝的品质,结合本研究结果,建议将水分、总灰分、酸不溶性灰分和水溶性浸出物(热提法)4项检查均纳入各省绞股蓝药材质量控制项目,拟定绞股蓝药材标准中水分限量为不高于12.0%,总灰分含量不高于16.0%,酸不溶性灰分不高于3.0%,热浸法所得水溶性浸出物含量不低于25.0%。在此限量标准下,本研究中符合要求的供试样品为安徽、福建、陕西和湖南各1批次,其他批次不合格的主要原因为总灰分和酸不溶性灰分超过限量。建议在绞股蓝药材生产过程中规范生产技术、保存得当,以保证绞股蓝药材的质量。
3.2 茶饮绞股蓝质量控制标准代用茶是由可用于食用的植物花、叶、果、根等为原料加工制成,应当符合《NYT2140-2015绿色食品代用茶》标准,其中规定叶类的水分含量低于7.5%,灰分含量低于12%[30],但在本试验55批次茶饮绞股蓝中,水分达标的仅14批次,不合格率为74.5%,达标的样品中8批次来源于陕西,2批次来源于湖北,各占对应省份总样品的57.1% 和66.7%,其他省份的样品几乎都不达标;总灰分共有19批次合格,不合格率为65.5%,其中陕西11批,湖南和湖北各2批;陕西、湖北和福建茶饮绞股蓝的浸出物含量较其他省份样品更高。目前,关于绞股蓝茶的相关标准主要为陕西、广西和江西发布的《DB36T 1264-2020绞股蓝规范化生产技术规程》《DB45T 2046-2019地理标准产品金秀绞股蓝茶》《DB61T 931.5-2014绞股蓝茶采摘技术规范》《DB61T 931.6-2014绞股蓝茶加工技术规范》《DB61T 931.7-2014绞股蓝茶》和《DBS61 0019-2019食品安全地方标准平利绞股蓝》 [31-36],其中平利绞股蓝有较为严格的理化指标限量,要求样品水分和灰分含量均较低。除陕西、广西和江西三省(区)外,其他省份未有绞股蓝茶的相关理化指标限制,故生产规范有待进一步提高。本研究通过对不同产地、不同部位的茶饮绞股蓝样品进行分析,发现含水量和浸出物存在不同,但总灰分和酸不溶性灰分差异较小。此外,各省区采用的标准不同,导致不同产地的茶饮绞股蓝质量差异较大,其中陕西、广西、湖北和福建等产地的茶饮绞股蓝浸出物含量较高,质量较好。结合茶饮绞股蓝现有的标准和本研究结果,建议建立全国性统一的茶饮绞股蓝质量控制标准,对绞股蓝的开发利用将具有较大提升。
4 结论我国现有的5个省(区)绞股蓝药材质量控制项目设置,已不能满足目前的市场需求。本研究采用《中国药典》通则项下方法测定不同产地绞股蓝的水分、灰分、水溶性浸出物含量,结合研究结果建议将水分、总灰分、酸不溶性灰分和水溶性浸出物(热提法)4项检查设置为各省绞股蓝药材质量控制项目,拟定药用绞股蓝水分、总灰分含量分别不得超过12.0%、16.0%,酸不溶性灰分含量不高于3.0%,水溶性浸出物(热浸法)含量不低于25.0%。结合陕西、广西和江西三省(区)绞股蓝茶的相关质量控制标准和《NYT2140- 2015绿色食品代用茶》标准,建议依据茶饮绞股蓝使用部位的不同制定或细化相应质量控制或标准,建立全国性统一的茶饮绞股蓝标准,进一步提高绞股蓝的生产技术规范。
| [1] |
中国科学院中国植物志编委会. 中国植物志[M]. 北京: 科学出版社, 1986. Editorial Committee of Flora of China, Chinese Academy of Sciences. Flora of China[M]. Beijing: Science Press, 1986: 269. |
| [2] |
边古筝, 禹玉华, 郁书君, 熊秉红, 陈颖, 刘仁昌. 药用植物绞股蓝研究进展[J]. 农业与技术, 2014, 34(2): 1-5. DOI:10.3969/j.issn.1671-962X.2014.02.003 BIAN G Z, YU Y H, YU S Z, XIONG B H, CHEN Y, LIU R C. Progress in the medicinal plant Gynostemma[J]. Agriculture and technology, 2014, 34(2): 1-5. DOI:10.3969/j.issn.1671-962X.2014.02.003 |
| [3] |
黄盼盼. 绞股蓝药材与配方颗粒质量标准研究[D]. 杭州: 浙江中医药大学, 2019. HUANG P P. Study on quality standard of Gynostemma pentaphyllum and formula granules[D]. Hangzhou: Zhejiang University of Traditional Chinese Medicine, 2019. |
| [4] |
沈子琳, 王振波, 侯会芳, 张莉, 黄建军. 绞股蓝的化学成分和药理作用及应用研究新进展[J]. 人参研究, 2020, 32(5): 59-64. DOI:10.19403/j.cnki.1671-1521.2020.05.015.v SHEN Z L, WANG Z B, HOU H F, ZHANG L, HUANG J J. Research progress on chemical constituents, pharmacological action and application of Gynostemma pentaphylum[J]. Ginseng Research, 2020, 32(5): 59-64. DOI:10.19403/j.cnki.1671-1521.2020.05.015.v |
| [5] |
LING Y, LEI Z N, LI X Y, YAN X Y, WANGS Y, YANG W L, NIE Q H, ZHANG Q, BAO H O, YU J M, JIN H G. Characterization and identification of the chemical constituents of Gynostemma pentaphyllum using High Performance Liquid Chromatography – Electrospray Ionization – Quadrupole Time-of-Flight Tandem Mass Spectrometry (HPLC-ESI-QTOF-MS/MS)[J]. Analytical Letters, 2020, 53(5): 761-773. DOI:10.1080/00032719.2019.1675075 |
| [6] |
WANG Z C, WANG Z, HUANG W H, SUO J M, CHEN X T, DING K Q, SUN Q, ZHANG H R. Antioxidant and anti-inflammatory activities of an anti-diabetic polysaccharide extracted from Gynostemma pentaphyllum herb[J]. International Journal of Biological Macromolecules, 2020, 145: 1-23. DOI:10.1016/j.ijbiomac.2019.12.213 |
| [7] |
MAN L, WANG Y R, ZHAI X F, XING S F, PIAO X L. Protective effects of flavonoids from Gynostemma pentaphyllum on oxidative damage in LLC-PK1 cells[J]. China Journal of Chinese Materia Medica, 2019, 44(6): 1193-1200. DOI:10.19540/j.cnki.cjcmm.20181226.019 |
| [8] |
ZHANG X S, SHI G H, WU X J, ZHAO Y Q. Gypensapogenin H from hydrolyzate of total Gynostemma pentaphyllum saponins induces apoptosis in human breast carcinoma cells[J]. Natural product research, 2018, 34(11): 1-5. DOI:10.1080/14786419.2018.1525370 |
| [9] |
SHEN C Y, MA P Y, ZHU J J, JIANG J G, LIU L, YI Y K, ZHU H X, LIU Q. Saponin extracts from Gynostemma pentaphyllum(Thunb.)Makino display sedative-hypnotic and anxiolytic effects[J]. Industrial Crops and Products, 2020, 157: 1-11. DOI:10.1016/J.INDCROP.2020.112893 |
| [10] |
YIN M J, ZHANG J J, WANG L Z, LI F Y, LI Z F, XIANG W, BIE S T, WANG C H, LI Z. Ten new dammarane-type saponins with hypolipidemia activity from a functional herbal tea-Gynostemma pentaphyllum[J]. Molecules(Basel, Switzerland), 2020, 25(16): 1-19. DOI:10.3390/molecules25163737 |
| [11] |
WANG B L, NIU J F, MAI B J, SHI F Y, LI M, CHEN L J, WANG P, LIU Q H. Effects of extraction methods on antioxidant and immunomodulatory activities of polysaccharides from superfine powder Gynostemma pentaphyllum Makin[J]. Glycoconjugate Journal, 2020. DOI:10.1007/s10719-020-09949-5 |
| [12] |
熊颖, 李纯, 任晋, 栗建明, 顾利红. SPE-LC-MS/MS和SPE-GCMS/MS测定绞股蓝中109种农药残留[J]. 中南药学, 2018, 18(12): 2044-2049. XIONG Y, LI C, REN J, LI J M, GU L H. Etermination of 109 pesticide residues in Gynostemma pentaphyllum by SPE-LC-MS/MS and SPE-GC-MS/MS[J]. Central South Pharmacy, 2018, 18(12): 2044-2049. |
| [13] |
景文祥, 练东明, 姜勇, 高会彬, 周成强. 石墨炉原子吸收法测定绞股蓝茶中铅含量[J]. 食品工业, 2018, 39(3): 306-308. JING W X, LIAN D M, JING Y, GAO H B, ZHOU C Q. Determination of lead in Gynostemma pentaphyllum tea by graphite furnace atomic absorption spectrometry[J]. 2018, 39(3): 306-308. |
| [14] |
王志强, 苏静. 石墨炉原子吸收光谱法测定绞股蓝中的重金属含量[J]. 化工管理, 2018(15): 72-73. DOI:10.3969/j.issn.1008-4800.2018.15.058 WANG Z Q, SU J. Determination of heavy metal in Gynostemma using graphite furnace atomic absorption spectrometry[J]. Chemical Enterprise Management, 2018(15): 72-73. DOI:10.3969/j.issn.1008-4800.2018.15.058 |
| [15] |
张子龙, 李雯珊, 滕菲, 匡艳辉, 范冬冬, 王德勤, 朱晶晶, 王智民. 绞股蓝总苷提取物及总苷片的质量标准研究[J]. 中国中药杂志, 2020, 45(24): 5976-5981. ZHANG Z L, LI W S, TENG F, KUANG Y H, FAN D D, WANG D Q, ZHU J J, WANG Z M. Study on quality standard of gypenosides extract and gypenosides tablets[J]. China Journal of Chinese Materia Medica, 2020, 45(24): 5976-5981. |
| [16] |
曲乐婧. 绞股蓝配方颗粒及其质量标准的研究[D]. 西安: 西北大学, 2020: 47-55. QU L J. Study on Gynostemma pentaphyllum dispensing granule and its quality standard[D]Xi'an: Northwest University, 2020: 47-55. |
| [17] |
傅泉炎. 中药含水量与中药仓储质量的关系[J]. 中国药业, 2002(5): 70. DOI:10.3969/j.issn.1006-4931.2002.05.052 FU Q Y. Relationship between water content and storage quality of traditional Chinese Medicine[J]. China Pharm, 2002(5): 70. DOI:10.3969/j.issn.1006-4931.2002.05.052 |
| [18] |
郝小佳. 中药材储藏方法和影响因素探析[J]. 临床医药文献电子杂志, 2020, 7(35): 174-175. DOI:10.16281/j.cnki.jocml.2020.35.140.jocml.2020.35.140 HAO X J. Analysis on storage methods and influencing factors of Chinese medicinal materials[J]. Electronic Journal of Clinical Medicine Literature, 2020, 7(35): 174-175. DOI:10.16281/j.cnki.jocml.2020.35.140.jocml.2020.35.140 |
| [19] |
四川省食品药品管理局. 四川省中药材标准[M]. 成都: 四川科学技术出版社, 2011. Sichuan Food and Medical Products Administration. Sichuan Chinese materia medica standards[M]. Chengdu: Sichuan Science and Technology Press, 2011. |
| [20] |
江西省卫生厅编. 江西省中药材标准[M]. 南昌: 江西科学技术出版社, 1996. Health commission of Jiangxi Province. Jiangxi Chinese materia medica standards[M]. Nanchang: Jiangxi Science and Technology Press, 1996. |
| [21] |
宁夏食品药品监督管理局. 宁夏中药材标准[M]. 银川: 阳光出版社, 2018. Ningxia Food and Medical Products Administration. Ningxia Chinese materia medica standards[M]. Yinchuan: Sunshine Press, 2018. |
| [22] |
贵州省药品监督管理局. 贵州省中药材、民族药材质量标准[M]. 贵阳: 贵州科技出版社, 2003. Guizhou Food and Medical Products Administration. Guizhou Chinese and ethnic materia medica standards[M]. Guiyang: Guizhou Science and Technology Press, 2003. |
| [23] |
广西壮族自治区食品药品监督管理局. 广西壮族自治区瑶药材质量标准[M]. 南宁: 广西科学技术出版社, 2014. Guangxi Zhuang Autonomous Region Food and Medical Products Administration. Guangxi Zhuang Autonomous Region Chinese materia medica standards[M]. Nanning: Guangxi Science and Technology Press, 2014. |
| [24] |
福建省食品药品监督管理局. 福建省中药材标准[M]. 福州: 海风出版社, 2006. Fujian Food and Medical Products Administration. Fujian Chinese materia medica standards[M]. Fuzhou: Haifeng Press, 2006. |
| [25] |
中华人民共和国香港特别行政区卫生署. 香港中药材标准(第五册)[M]. 香港: 中华人民共和国香港特别行政区卫生署出版社, 2012. Department of Health, Hong Kong Special Administrative Region of the People's Republic of China. Hong Kong Chinese materia medica standards(5th Volume)[M]. Hong Kong: Department of Health Press of Hong Kong Special Administrative Region of the People's Republic of China, 2012. |
| [26] |
山西省食品药品监督管理局. 山西省中药材中药饮片标准[M]. 北京: 科学出版社, 2014. Shanxi Food and Medical Products Administration. Shanxi Province Standards for Chinese medicines material and Chinese herbal pieces[M]. Beijing: Science Press, 2014. |
| [27] |
山东省食品药品监督管理局. 山东省中药材标准[M]. 济南: 山东科学技术出版社, 2012. Shandong Administration for Food and Medical Products. Shandong Chinese materia medica standards[M]. Jinan: Shandong Science and Technology Press, 2012. |
| [28] |
湖南省食品药品监督管理局. 湖南省中药材标准[M]. 长沙: 湖南省科学技术出版社, 1993. Hunan Food and Medical Products Administration. Hunan Chinese materia medica standards[M]. Changsha: Hunan Science and Technology Press, 1993. |
| [29] |
湖北省食品药品监督管理局. 湖北省中药材标准[M]. 武汉: 湖北科学技术出版社, 2009. Hubei Food and Medical Products Administration. Hubei Chinese materia medica standards[M]. Wuhan: Hubei Science and Technology Press, 2009. |
| [30] |
中华人民共和国农业部. 绿色食品代用茶: NYT2140-2015[S]. 北京: 2015. Ministry of Agriculture of the People's Republic of China. Green food substitute tea: NYT2140-2015[S]. Beijing, 2015. |
| [31] |
陕西省卫生健康委员会. 食品安全地方标准平利绞股蓝: DBS61 0019-2019[S]. 陕西, 2019. Health Commission of Shaanxi Province. Local standard for food safety Pingli County Gynostemma: DBS61 0019-2019[S]. Shaanxi, 2019. |
| [32] |
陕西省质量技术监督局. 绞股蓝茶: DB61T 931.7-2014[S]. 陕西, 2014. Shaanxi Quality and Technical Supervision Bureau. Gynostemma tea: DB61T 931.7-2014[S]. Shaanxi, 2014. |
| [33] |
陕西省质量技术监督局. 绞股蓝茶加工技术规范: DB61T 931.6- 2014[S]. 陕西, 2014. Shaanxi Quality and Technical Supervision Bureau. Technical specification for Gynostemma Tea processing: DB61T 931.6-2014[S]. Shaanxi, 2014. |
| [34] |
陕西省质量技术监督局. 绞股蓝茶采摘技术规范: DB61T 931.5- 2014[S]. 陕西: 2014. Shaanxi Quality and Technical Supervision Bureau. Technical specifications for picking Gynostemma tea: DB61T 931.5-2014[S]. Shaanxi: 2014. |
| [35] |
广西壮族自治区市场监督管理局. 地理标准产品金秀绞股蓝茶: DB45T 2046-2019[S]. 广西, 2019. Guangxi Zhuang Autonomous Region. Administration for Market Regulation. Product of geographical indications--Jinxiu Gynostemma tea: DB45T 2046-2019[S]. Guangxi, 2019. |
| [36] |
江西省市场监督管理局. 绞股蓝规范化生产技术规程: DB36T 1264-2020[S]. 江西, 2020. Jiangxi Administration for Market Regulation. Technical regulations for standardized production of Gynostemma pentaphyllum: DB36T 1264- 2020[S]. Jiangxi, 2020. |
 2021, Vol. 48
2021, Vol. 48